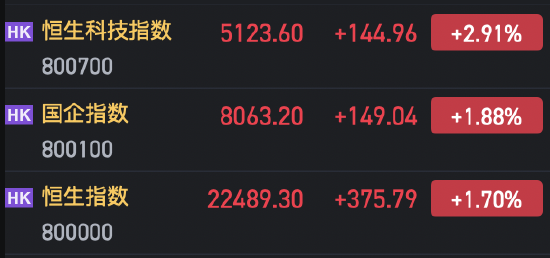
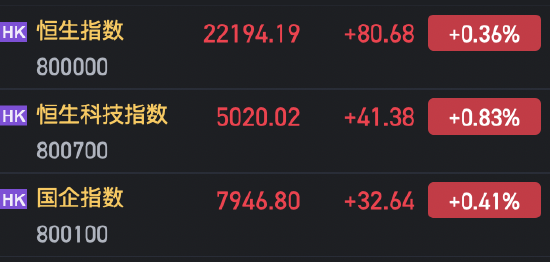
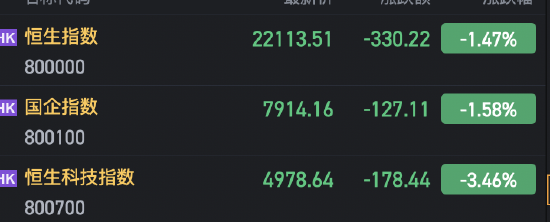
全球首個口服司美格魯肽在華獲批,GLP-1藥物市場或生變局
近日,國家藥品監督管理局(NMPA)發佈最新藥物批準文件,諾和諾德開發的司美格魯肽片正式獲批在中國上市,用於治療2型糖尿病患者,這是國內首個獲批上市的口服GLP-1受體激動劑。司美格魯肽因其“減肥神藥”的稱號為人們所熟知,也為諾和諾德帶來大幅業績增長。
司美格魯肽雖還未在中國獲批減重適應症,但在實際使用中被大量用於減肥。目前國內獲批減肥的GLP-1藥物包括華東醫藥的利拉魯肽及仁會生物的貝那魯肽,在研臨床產品多為給藥次數更少的長效製劑,以及具有口服優勢的小分子藥物。據相關消息透露,司美格魯肽片減重相關的適應症已在中國啟動III期臨床試驗。此外,禮來的替爾泊肽進入中國市場也迎來倒計時,這款藥物被稱為司美格魯肽當今最大的競爭對手。
此次口服司美格魯肽獲批或給我國GLP藥物和減重市場帶來新的變局。招商健康投資總監劉侃在接受21世紀經濟報導記者採訪時表示,由於需要多種換算以及嚴格的服用時間要求等因素,目前,諾和諾德司美格魯肽口服製劑的患者依從性相對較差。因此,短期來看,口服司美格魯肽上市對市場的影響有限,但長期而言,隨著技術的不斷更新,口服製劑患者依從性不斷提高是發展方向。
圖片來源:IC photoGLP-1市場競爭格局或生變
1月26日,NMPA批準了諾和諾德公司研發生產的諾和忻®(司美格魯肽片)在中國的上市申請,用於成人2型糖尿病治療。這是國內首個獲批上市的口服GLP-1受體激動劑。據諾和諾德介紹,作為全球首個且目前唯一GLP-1片劑,諾和忻®的口服便利性,可強效降糖,兼具多重代謝獲益,助力患者提升治療依從性。
在全球,諾和諾德目前共有三款司美格魯肽產品在售,包括用於降糖的皮下注射製劑Ozempic、用於降糖的口服片劑Rybelsus,以及減重產品Wegovy。此前,2021年4月,NMPA已批準司美格魯肽注射液Ozempic(諾和泰®)在中國的上市申請。
司美格魯肽為諾和諾德帶來大幅業績增長。財報數據顯示,諾和諾德2023年前三個季度的銷售額累計達1663.98億丹麥克朗,同比增長29%。三款司美格魯肽產品的銷售額合計達約1002億丹麥克朗,占該公司整體銷售額60%以上。
自司美格魯肽注射液在華獲批後,其銷量增長迅猛,根據諾和諾德公告,中國地區2023年前三季度Ozempic實現收入38.13億丹麥克朗(約40.03億人民幣),同比增長160%。其中第三季度實現收入16.00億丹麥克朗(約16.80億人民幣),同比增長167%,在按地域劃分的市場中增速最快。
除司美格魯肽外,銷量快速增長的GLP-1類藥物還有禮來的替爾泊肽(Tirzepatide),這款藥物被稱為司美格魯肽當今最大的競爭對手。2022年5月替爾泊肽注射液獲FDA批準用於治療2型糖尿病;2023年11月8日,替爾泊肽注射液減重適應症獲得FDA批準。
根據禮來財報,2023年前三季度替爾泊肽全球銷售額達29.58億美元,其中第三季度全球銷售為14.09億美元。國金證券研報介紹,替爾泊肽在上市後第六個季度便實現單季度銷售額突破10億美元,目前在美國GLP-1藥物市場中處方占比已經上升至19.5%,崛起趨勢強勁。
由於GLP-1受體激動劑安全有效,目前已成為減肥藥物臨床研究的核心靶點,近年來GLP-1藥物市場增長迅速。根據弗若斯特沙利文數據,全球GLP-1市場規模從2016年的52億美元增長至2021年的154億美元,2016—2021年年復合增長率為24.3%,預計2025年達283億美元,預計2021年—2025年年復合增長率達16.4%。
在國內市場方面,弗若斯特沙利文數據顯示,中國GLP-1市場規模從2016年的4億元增長至2021年的27億元,2016—2021年年復合增長率為46.5%,預計2025年達156億元,預計2021—2025年年復合增長率達55.0%。
當前,國內也有多家企業佈局GLP-1/GLP-1R激動劑,據德邦證券研報數據,截至2023年6月14日,國內已經申請臨床及以上的GLP-1類藥物一共99個。除禮來、諾和諾德等國外巨頭進軍國內GLP-1市場外,國內藥企也搶灘登陸持續發力,目前華東醫藥、恒瑞醫藥在GLP-1類新藥數量上領跑國內藥企。
此次口服司美格魯肽獲批將如何影響我國GLP-1藥物市場競爭格局?劉侃向21世紀經濟報導記者表示,實際上,由於需要多種換算以及嚴格的服用時間要求等因素,相對於諾和諾德司美格魯肽注射液而言,口服製劑的患者依從性及方便程度相對較差。參考口服司美格魯肽在海外獲批後的市場情況,根據諾和諾德2023年三季度報告,皮下注射製劑Ozempic的銷售金額遠高於降糖口服片劑Rybelsus。
不過同時,劉侃也認為,隨著技術的不斷更新,口服製劑的使用方式會更加便利,患者依從性也會逐漸提高,口服藥物推廣的大方向是正確的。“因此,短期來看,口服司美格魯肽上市對市場的影響有限,但長期而言,患者依從性不斷提高是發展方向。”
此外,從消費端而言,劉侃也指出,口服司美格魯肽的推廣還會面臨產能方面的問題。此前,因為銷售太過火爆,不少國家出現司美格魯肽供應短缺狀態,多國紛紛限制了司美格魯肽的使用。
劉侃介紹,由於需要經過胃和腸道進行消化吸收,口服藥物的生物利用度遠低於注射藥物,司美格魯肽口服製劑與注射製劑的生物利用度可能會相差10—20倍。因此,在口服司美格魯肽上市後,還需要一系列提高產能的配套措施。爭奪減重市場
司美格魯肽更為人們所熟知的是其“減肥神藥”的稱號,雖還未在中國獲批減重適應症,但在實際使用中已被大量用於減肥。當前,超重及肥胖人數上升驅動全球及中國減重藥市場高速發展。
根據弗若斯特沙利文數據,全球減重藥市場規模預計2030年達115億美元,預計2023—2030年年復合增長率為14.7%。在中國減重藥市場規模方面,弗若斯特沙利文數據顯示,中國減重藥市場規模2016年—2023年年復合增長率為56.2%,預計2030年達149億人民幣,預計2024—2023年年復合增長率為12.4%。
在2023年6月,諾和諾德向中國藥監部門提交了司美格魯肽注射液新適應症的上市申請,據業界猜測,此次申報的適應症很可能為萬眾期待的減重適應症。另據相關消息透露,口服司美格魯肽片減重相關的適應症已在中國啟動III期臨床試驗。
在國內減重藥市場方面,德邦證券研報介紹,目前國內獲批減肥的GLP-1藥物包括華東醫藥的利拉魯肽及仁會生物的貝那魯肽,在研臨床產品多為給藥次數更少的長效製劑,以及具有口服優勢的小分子藥物。
當前,禮來的替爾泊肽進入中國的時間也進入倒計時,2023年8月21日,NMPA正式受理了禮來替爾泊肽適應症用於成人減重的上市申請,目前正在審評中。
除司美格魯肽和替爾泊肽外,值得關注的還有禮來與信達生物合作研發的GLP1R/GCGR雙重激動劑瑪仕度肽。2023年12月26日,CDE藥物臨床試驗登記與信息公示平台顯示,信達生物啟動了瑪仕度肽頭對頭司美格魯肽III期臨床試驗。信達生物此前表示,預計在2023年末至2024年初提交瑪仕度肽上市申請。
在此次口服司美格魯肽獲批的三天前,1月23日,諾和諾德與EraCal Therapeutics達成合作和許可協議,以開發和商業化EraCal開發的針對控製食慾和體重的新型作用機制口服小分子,以鞏固其在重磅市場的領先地位。根據協議,諾和諾德將獲得開發和商業化該項目的獨家權利,而EraCal有資格獲得高達2.35億歐元的預付款、開發和商業里程碑,以及產品上市銷售後的版稅。
有行業觀點指出,諾和諾德引入該項目的舉動進一步推動了自與EraCal開展源頭新藥研究合作以來已形成的業務發展戰略。在此期間,諾和諾德收購了Embark Biotech和Inversago Pharma,與Omega Therapeutics達成了合作,並在其他方面為產品管線奠定了基礎。
對於諾和諾德的一系列收購動作,劉侃認為,這體現了諾和諾德戰略佈局的深謀遠慮,藥企需要考慮其管線的排放梯度和節奏感,熱銷產品、研發後端、儲備管線等都需要有所佈局。
當前,司美格魯肽藥物銷售十分火爆,但劉侃也指出,在競爭激烈的GLP-1賽道中諾和諾德仍面臨一些挑戰,例如替爾泊肽、瑪仕度肽等雙靶點藥物的出現,以及在研的三靶點藥物。“當前,禮來的替爾泊肽已擺出‘死磕’降糖、減重領域的決心,與市面主流產品開展了9項頭對頭適應症研究,有7項研究替爾泊肽治療效果均好於市面主流產品,其中就包括司美格魯肽。”
“面對當前暢銷的產品,諾和諾德並沒有躺在功勞簿上,而是認真考慮當前激烈的市場競爭,進行長遠佈局。”劉侃表示。