AI輔助雪藏電鏡解析纖毛結構,浙大學者構建候選致病基因庫,提供纖毛病研究新思路

纖毛是在真核細胞表面廣泛分佈的一種細胞器,它賦予細胞運動和感知外界信號的能力。一個細胞可以有一根(如精子)或幾百根纖毛(如呼吸道上皮纖毛細胞),當編碼纖毛成分的基因發生遺傳突變或纖毛結構缺失時,通常會引發纖毛病。
纖毛病是一大類遺傳病,發病率約為 1/1000,涉及因纖毛功能障礙引起的生殖不育、反復呼吸系統感染、內臟異位等全身多器官異常。
長久以來,纖毛病的臨床分子診斷和治療一直是難點所在。此前,傳統方法通過對臨床病例進行基因測序及數據分析,可以鑒定出一些致病基因。但仍有大量致病基因未被發掘,且基因突變如何引起纖毛組裝和運動缺陷的機制尚不清楚。這些問題的背後主要是纖毛作為一種大型細胞器,其具體分子組成和組裝機制尚未被完整解析。
浙江大學良渚實驗室研究員桂淼專注於運用雪藏電鏡和 AI 輔助原子建模明確纖毛類細胞器核心骨架的分子組成、構建候選致病基因庫並應用於纖毛病診療等。這些工作建立了纖毛病研究的新範式,也對未來其他細胞器相關疾病的研究具有推廣意義。近期,憑藉在該領域取得的突破性進展,他入選了 2023 年度《麻省理工科技評論》中國區「35 歲以下科技創新 35 人」。
 圖 | 桂淼研究員
圖 | 桂淼研究員桂淼在北京大學基礎醫學院獲得生物物理學博士學位,後在清華大學和哈佛醫學院從事博士後研究工作,曾任哈佛醫學院生化與分子藥理系講師。加入浙江大學組建獨立實驗室後,重點關注纖毛的結構蛋白組學和結構遺傳學,由於纖毛與精子運動的緊密聯繫,還拓展了生殖醫學這一新方向,希望利用在結構生物學上的發現為不孕不育等問題提供新見解。

構建纖毛領域的「人類基因組計劃」,指導纖毛病的臨床診治
「於我而言,利用雪藏電鏡解析和觀察生物體結構這種直觀理解生命的方法很有意義,這激發了我的學習興趣,我非常看好雪藏電鏡在生物醫學研究中的應用。」桂淼回憶道。
他在結構生物學領域已深耕多年,並取得了多項重要進展。博士期間,桂淼主要關注囊膜病毒表面糖蛋白的結構,首次解析了 SARS-CoV-1 刺突蛋白及其與受體 ACE2 復合物結構,發現了刺突受體結合域的多種構象;還揭示了伊波拉病毒中和性抗體的作用機制。
後續,在海外留學期間,他進一步擴展了之前的工作,開始重點關注細胞骨架和纖毛等方向。隨著對結構生物學的深入理解,桂淼意識到雪藏電鏡有潛力挖掘細胞內更多未知的奧秘。他開始從結構生物學視角出發、以蛋白質為切入點,通過深度解析纖毛結構,探索開發纖毛病臨床診治的新方法。
「不過,要想真正實現這一點並不容易。不同於傳統單個生物分子的結構解析,纖毛是真核細胞內最大的分子機器之一,其分子組成極其複雜且未知。」桂淼說。
在此背景下,桂淼建立了一套基於雪藏電鏡結構解析和 AI 結構預測的快速精準蛋白質鑒定和原子模型搭建方法,近乎完整解析了包含 400 萬個原子的纖毛軸絲的三維結構,併成功鑒定出超 200 種纖毛組成的蛋白質,包括幾十種定位和功能未知的蛋白質。
 (Walton and Gui et al., Nature)
(Walton and Gui et al., Nature)(來源:受訪者提供)
基於已解析的纖毛結構,纖毛病的診治產生了新思路。他解釋道,「此前的診斷方法主要是從臨床出發自上而下鑒定致病基因,即從臨床病例出發,採用基因測序等手段篩選致病基因。我們的方法與此不同,在結構解析時,我們發現,組成纖毛的 200 多個蛋白質中任何一個突變都可能導致纖毛相關疾病,並能基於結構直觀理解其致病機制,這是一種自下而上發掘纖毛病致病基因的新思路。」
通過全面解析纖毛結構,並結合生物學手段驗證及整理致病基因,從而構建比較完整的候選致病基因庫。在此基礎上,只需對病人進行基因測序,篩查纖毛突變基因,如果突變在致病基因庫中即可以判斷是否該突變基因導致了疾病發生。這大大簡化了診斷過程,提高了纖毛病分子診斷的準確性,也方便了臨床篩查。桂淼說:「這種研究思路更加高效,並能直觀基於結構闡明致病機制,也能為纖毛病的臨床診治提供更高效的方法。」 不過,他同時也指出,儘管理論上這些基因突變具有潛在致病性,但還需要結合臨床數據及生物學實驗驗證這些基因突變與臨床症狀的直接因果關係及其致病機制,以進一步提高診療的準確性。
目前,該致病基因庫已被公開提供給國內外相關領域的研究人員。桂淼表示,無論是應用於基礎研究還是臨床篩查,基因庫都得到了廣泛的認可和好評。這種新方法一方面可以幫助研究人員從原子水平理解纖毛的組裝和運動這些細胞生物學的基本問題;另一方面建立了纖毛病研究的新範式,也被領域內專家類比為纖毛研究領域的「人類基因組計劃」。
值得一提的是,桂淼和浙江大學的同事還依託浙江大學良渚實驗室和醫學院附屬兒童醫院等優秀的臨床和科研平台,組成了集臨床醫生、細胞生物學家和結構生物學家在內的立體合作團隊。該團隊開設了全國第一家纖毛病門診和科研平台,希望進一步提高纖毛的基礎和臨床研究。
「我們的終極目標是基於結構和功能研究深入挖掘男性弱精症和原發性纖毛運動障礙等纖毛相關疾病的新致病基因和發病機制,並將這些研究範式推廣到其他系統,包括先天性侏儒症和小頭症等中心體相關疾病。」

「纖毛病研發還處於產業化早期階段」
纖毛病是由於纖毛功能異常或結構缺陷引起的多系統遺傳性疾病,患者常會出現反復慢性呼吸道感染、腎臟疾病、心臟病、不孕症等,嚴重時甚至危及生命。
據統計,目前已發現超過 20 種纖毛病,還有更多纖毛相關疾病等待發掘。臨床的治療方法主要以緩解為主,還沒有獲批的相關療法可供患者使用。
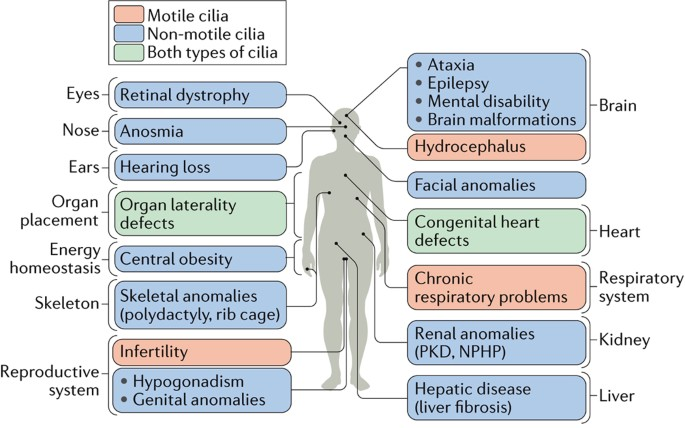 (來源:Nature Reviews Molecular Cell Biology)
(來源:Nature Reviews Molecular Cell Biology)「事實上,治療纖毛病還存在多個難點,首先,纖毛病的症狀很容易和其他疾病混淆,臨床診斷困難。另一方面,纖毛病的致病基因尚不完全清楚,致病機制複雜,這同樣對開發藥物提出了挑戰。」桂淼說。
基因治療通過直接靶向操作遺傳物質干預疾病的發生和發展,被視為從根本上治癒難治性和遺傳性疾病的有效手段。經過多年的發展,基因治療已經取得了越來越多重要的進展,多款基因藥物獲批上市。據統計,從 2012 年僅有 1 款基因療法獲批,到僅 2023 年就有 5 款基因療法/基因編輯療法獲 FDA 批準上市。預計未來十年,預計還將會有 40 多種新療法獲批。
不過,桂淼指出,對於由單一基因突變引起的疾病,可以通過導入正常基因進行基因治療,從而緩解疾病。然而,纖毛病涉及的基因種類繁多,導致基因治療的藥物可能只能對某些特定的纖毛病患者群體有效。長期來看,纖毛疾病需要更個性化的治療,實施難度較大,目前國外在該領域已有相關試驗性的開發。
公開資料顯示,成立於 2015 年的 Recode Therapeutics 是一家 mRNA 和基因治療公司,專注於開髮針對原發性纖毛運動障礙和囊性纖維化等遺傳疾病的 mRNA 和基因療法。目前已開發出 RCT1100 ,這是一種在研的 mRNA 吸入候選療法,用於治療由 DNAI1 (一編碼纖毛運動必需蛋白質的基因)致病突變引起的原發性纖毛運動障礙,有望能夠恢復肺部纖毛功能,從根本上解決疾病。該療法已於今年 6 月獲得美國 FDA 孤兒藥資格認定。
桂淼進一步提到,目前整個纖毛病領域的產業化還處在早期階段,相比較而言,國內的纖毛研究處於更早期階段,還有很多工作需要完成,不過相信未來我們能在纖毛病的診治上取得進一步突破。此外,通過普及纖毛和纖毛病相關的科普知識,可以讓公眾和臨床醫生瞭解這類疾病,早期發現和干預對控制疾病的進展非常重要,也許不久的將來就等到了有藥可用的那天。