科學家開發新型多光子顯微鏡,可實現大腦最深層皮層的大視野成像,定製組件已實現商品化
近日,美國康奈爾大學團隊開發出一種新型多光子顯微鏡——DEEPscope。
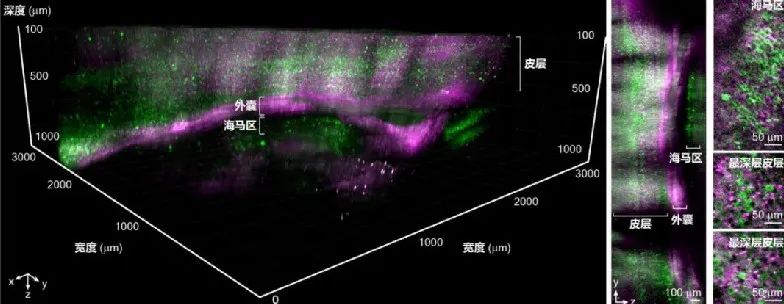
通過定製的全光學系統和大口徑多邊形掃瞄儀,以及結合激光自適應激發技術,DEEPscope 能夠實現亞微米解像度,並能實現 1mm 深度的結構成像,成像範圍涵蓋小鼠的所有大腦皮層和部分海馬區。
在三光子腦成像中,DEEPscope 能夠大大提升成像速度和成像廣度,能以 4Hz 的幀率實現 3.23×3.23mm² 的大視野成像。
除能拓寬光子成像的深度和廣度之外,通過優化多光子螢光信號的生成效率,DEEPscope 還能克服雙光子成像深度和三光子成像視野的限制,從而能夠實現深層大視野成像。
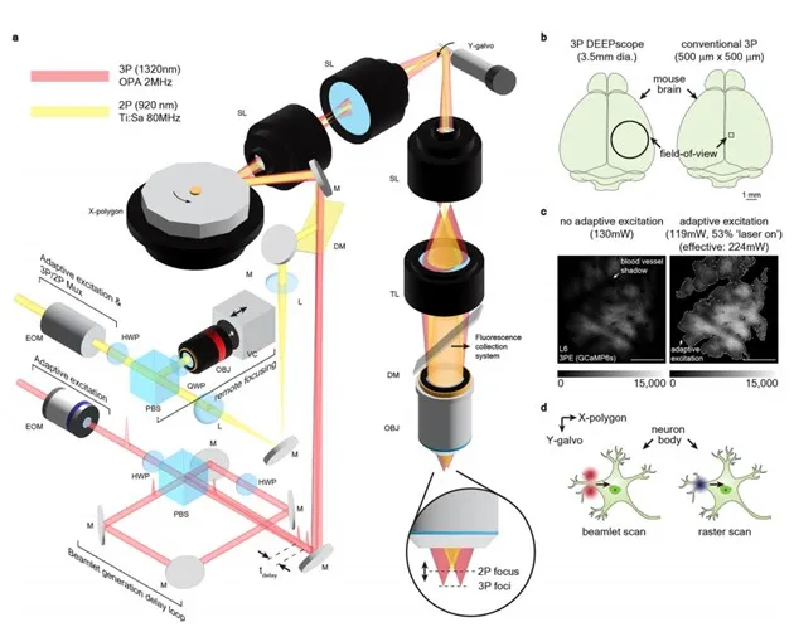 (來源:eLight)
(來源:eLight)此外,DEEPscope 採用多光束掃瞄方案和自適應激發系統,這讓其具有模塊化和可擴展的特點,故能大幅降低大視野多光子成像系統的複雜性,因此能夠集成到任何多光子顯微鏡中。
目前,DEEPscope 已能用於鼠腦和成體斑馬魚的大視野深層成像,這證明它在各種模型生物或組織樣本中也具有廣泛應用潛力,比如也能用於腫瘤和淋巴結的成像,從而能夠用於研究免疫細胞在淋巴結中的動態行為,以及用於觀測腫瘤微環境中的結構和細胞活動。
為了方便應用落地,研究人員採用供應商的定製模塊化方案,讓 DEEPscope 能夠實現高性能和便捷性的平衡。目前,這家供應商已經將這些定製組件加以商品化,因此用戶可以直接購買。
總的來說,DEEPscope 不僅能實現高效、快速和大視野的三光子成像,還能顯著擴展多光子顯微鏡的應用潛力,為實現多光子顯微鏡的大視野、深層次、高解像度成像提供了良好解決方案,並能被用於免疫學和神經科學等領域。

用大視野深度成像助力疾病研究
談及研究背景該團隊表示,一些神經系統疾病會損害記憶力和運動能力,並會嚴重降低生活質量。要想深入理解這些複雜疾病的機制,基礎性生物研究必不可少,而最直接的辦法就是觀察和追蹤實驗小鼠的神經元細胞活動。
然而,此前的成像技術依舊無法收集到足夠多和足夠好的數據,比如無法同時觀測深層神經元和大範圍神經元的活動。
要想理解神經系統的疾病機制,大視野深度成像可謂極為關鍵。近年來,隨著雙光子顯微鏡技術的發展,已讓神經活動的大視野記錄成為可能。然而,該類技術的成像深度仍然局限於淺表皮層。
針對深層皮層表面和深層皮層之下的海馬區區域中的神經元,儘管傳統三光子顯微鏡能夠對其進行成像,但其成像範圍依舊局限於幾百微米的小視野之內。
這是因為隨著成像深度的增加,激光能量也會增強。但是,過高的激光能量會導致生物組織溫度升高,從而引發組織損害(即熱損傷)。而通過縮小成像視野,則能減少所需的激光能量,從而降低熱損傷的風險。
要想解決深層大視野的成像瓶頸以及實現大視野三光子顯微鏡,就必須提高螢光信號生成的效率,只有這樣才能降低成像所需的激光能量。
基於上述觀察,課題組定下這樣一個目標:開發一種能夠同時實現深層次、高解像度和大視野成像的新型顯微鏡。
 (來源:eLight)
(來源:eLight) 「神經元像星星一樣閃爍」
「神經元像星星一樣閃爍」要想完成這一目標首先需要解決大視野成像中的一個關鍵挑戰:提高三光子成像的螢光激發效率。
為此,他們定製了多邊形掃瞄器和光學系統(包括掃瞄透鏡和物鏡管透鏡)。通過反復的實驗和調整,該團隊構建出了 DEEPscope。
完成硬件開發之後,其又針對 DEEPscope 進行性能驗證。針對速度、解像度和成像深度等關鍵參數進行表徵之後,表徵結果顯示 DEEPscope 在深層成像和大視野成像中具有優越性。
此外,他們還在小鼠和斑馬魚等模型生物中進行活體成像實驗,進一步驗證了 DEEPscope 的穩定性和實用性。
同時,課題組還針對成像數據加以深入分析,以便全面驗證 DEEPscope 的性能。
通過評估神經元的螢光信號亮度,其發現 DEEPscope 在深層組織中仍能保持較高的信噪比,借此展示了 DEEPscope 在激發效率優化上的有效性。
同時,研究人員還記錄了深層神經元的神經活動模式,這不僅清晰展示了神經元的動態過程,也為深入研究大腦活動提供了強有力的數據支持。
而 DEEPscope 的應用並非僅僅局限於小鼠模型,該團隊還將其擴展至斑馬魚成體腦的研究之中。
斑馬魚的實驗結果顯示:DEEPscope 能夠實現大視野範圍內的高解像度結構成像,這證明其在不同模型生物中具有廣泛的適用性。
實驗中,掃瞄器的同步、激光功率的調控、以及螢光信號的捕捉,都需要精準的參數配合。之所以要調試 DEEPscope 的參數,是為了在針對最深層皮層實現成像的同時,還能讓其保持大視野。
而最深層皮層位於小鼠的大腦深處,同時要想實現大視野就必須具備極高的螢光激發效率。
研究中,課題組在實驗室連續調試好幾個小時,期間他們反復嘗試不同的激光分佈模式。每當實驗失敗時,他們都會記錄下問題,重新分析光路和信號處理流程。
終於,屏幕上開始呈現出一片清晰的圖像——最深層皮層神經元活動,分佈在了一個前所未有的大視野範圍內。
這張圖像不僅展示了幾百個最深層皮層的神經元,還能展示出每個神經元的細節,研究人員形容這就像是打開了一扇通往腦深處的窗口。
作為本次項目的主導者,莫浚賢和王天宇這樣描述上述場景:「當時已是深夜,實驗室里一片安靜。
我們盯著屏幕,感到一種不可思議的滿足和興奮。這是第一次親眼看到 DEEPscope 所實現的大腦最深層皮層的大視野成像。」
「當看到圖像上活躍的神經元像星星一樣閃爍,我們覺得自己彷彿是一名宇航員在探尋神秘太空的奧秘。」其補充稱。
概括來說,他們在本次研究中引入了一系列創新:利用多光束掃瞄方案來提高螢光生成效率、利用自適應激發方式來降低所需的平均功率。
其中,多光束掃瞄方案通過將單個激光脈衝分成多個小光束來監測神經元活動,從而能夠顯著提高螢光信號生成效率,進而能夠降低激光功率。
自適應激發模塊則能將激光脈衝集中用於目標成像區域,從而可以進一步減少激光功率。
在傳統的多光子顯微鏡中,激光能量通常均勻分佈於整個樣本,這種方式會導致能量浪費,尤其在無需成像的區域會增加熱損傷的風險。
而這些創新讓三光子中每個激光脈衝的螢光生成得以優化,從而讓深層大視野成為可能。
而通過數據分析和性能驗證,課題組不僅展現了 DEEPscope 在神經科學研究中的核心優勢,還為它在其他生物醫學領域的潛在應用奠定了基礎。
圖 | 相關論文(來源:eLight)
 圖 | 從左到右:莫浚賢和王天宇(來源:資料圖)
圖 | 從左到右:莫浚賢和王天宇(來源:資料圖)本次項目由莫浚賢和王天宇共同設計主導,康奈爾大學教授 Chris Xu 擔任通訊作者 [1]。
其中,王天宇現任美國波士頓大學電子計算機工程系助理教授,主要研究實驗光學和人工智能交叉等方向。
 參考資料:
參考資料:1.Mok, A.T., Wang, T., Zhao, S.et al. A large field-of-view, single-cell-resolution two- and three-photon microscope for deep and wide imaging. eLight 4, 20 (2024). https://doi.org/10.1186/s43593-024-00076-4
運營/排版:何晨龍