追問|中國醫生在歐洲介紹全球首個先天性耳聾基因療法重大突破
·10月27日,舒易來醫生在第30屆歐洲基因和細胞治療學會年會上分享了基因治療藥物RRG-003的全球首批多例基因治療臨床試驗結果,其數據顯示,5例患者中4例患者治療後有明顯的聽力改善,並且耐受性和安全性良好。
 舒易來醫生在第30屆歐洲基因和細胞治療學會年會上作報告。受訪者供圖
舒易來醫生在第30屆歐洲基因和細胞治療學會年會上作報告。受訪者供圖視頻中,一個小男孩背對鏡頭,母親在他背後大喊了一聲,他轉過頭來……小男孩的父母在視頻畫面上標記,這是他接受基因療法RRG-003後的第28天。
近日,複旦大學附屬眼耳鼻喉科醫院(上海市五官科醫院)耳鼻喉科研究院副院長、遺傳性耳聾診治中心主任舒易來醫生在接受澎湃科技採訪時介紹,這個小男孩今年兩歲,患有先天性耳聾,接受治療已經6個月。據小男孩母親介紹,治療前,他對任何聲音都沒有反應,無論是鞭炮聲還是打雷聲。因為聽不見,之前他敲門都沒有敲出聲音,單純模仿敲門的動作。
男孩母親告訴舒易來團隊:“治療後並沒有立刻起效,第14天時,孩子還不會對聲音做出反應。我們很緊張。差不多一個月才看到效果,我們一家人激動得都哭了。”舒易來告訴澎湃科技:“我看到的時候,也覺得很欣慰、很開心。”
先天性耳聾,指因遺傳因素或母體妊娠過程、分娩過程中的異常造成的聽力障礙。患有先天性耳聾的兒童可能從小就無法接收到聲音的刺激,往往因聾致啞,既聽不見聲音,也無法說話。由中國聽力醫學發展基金會發佈的《中國聽力健康報告(2021)》顯示,中國新生兒耳聾發病率為1‰-3.47‰,每年新增耳聾新生兒約3萬人,其中遺傳因素致聾的比例達60%。
10月27日,舒易來在比利時布魯塞爾舉行的第30屆歐洲基因和細胞治療學會年會(ESGCT)上,向全球同行分享了團隊與上海鼎新基因科技有限公司(以下簡稱“鼎新基因”)聯合研發的基因治療藥物RRG-003的全球首批多例基因治療臨床試驗結果,其數據顯示,5例患者中4例患者治療後有明顯的聽力改善,並且耐受性和安全性良好。
鼎新基因負責該項目執行的科學家高凱瑜博士稱:“這是在中國上海自主完成的、全球第一項獲得療效的內耳基因治療和雙AAV載體的人體試驗(Frist in human),臨床意義重大,雙載體技術路線、內耳給藥、患兒聽力評估以及語言功能恢復均是世界級的開創性工作。”
或可改變無藥可治的局面
目前,全球尚無可治療感音神經性耳聾的藥物上市,主流的臨床干預方式是助聽器、人工耳蝸植入。人工耳蝸是模擬人類耳蝸工作原理的電子植入體,可以將聲音信號轉換為電信號,繞過損壞的耳蝸毛細胞,直接刺激耳蝸聽神經,將聲音信號發送到大腦里,使人產生聽覺。也就是說,人工耳蝸是用電極、芯片、編碼策略製造出來的電子音模擬人耳聽到的自然聲音。
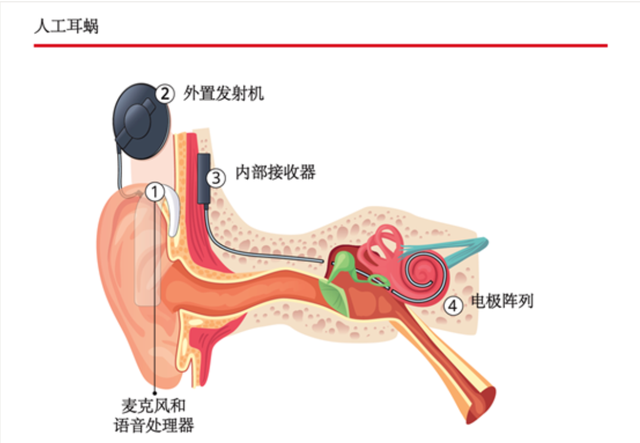 人工耳蝸。圖片來源:世界衛生組織《世界聽力報告》
人工耳蝸。圖片來源:世界衛生組織《世界聽力報告》既有人工耳蝸,為什麼還需要基因療法?據報導,人工耳蝸讓很多聾啞兒童回到了有聲世界,能與人交流,是聽覺領域重大的發明和創造。患者通過人工耳蝸聽到的聲音,要經過長期的訓練和學習這些“電波”的意義,而且在很多人同時說話或嘈雜環境中時,解像度會下降。再者,手術植入人工耳蝸後,患者需要在耳朵附近長期佩戴外機,外機關閉或沒電時,他們就聽不見了。
上海市五官科醫院耳鼻喉科主任李華偉教授表示,基因治療是針對病因的治療方法,患兒在接受基因治療後,聽見的聲音和普通人無異,而且從外表也看不出治療的痕跡。
“RRG-003是靶向OTOF基因的基因治療藥物。受試患者的OTOF基因有缺陷,無法正常地發揮作用,我們使用AAV載體將正常的基因注射到患者的耳朵裡,它可以產生正常蛋白,彌補患兒本身的基因缺陷,讓他們的聽覺重新恢復。”舒易來解釋。
OTOF基因編碼一種與囊泡釋放功能相關的“耳畸蛋白”。該基因突變可導致耳畸蛋白功能缺陷從而引起明顯的聽力障礙。過往的研究表明,OTOF是最有潛力率先實現耳聾治療臨床轉化的靶向基因。
在啟動人體臨床研究之前,舒易來在先天性耳聾基因療法研究的路上已經走了十多年。據其介紹,目前已有150多種基因被鑒定與先天性耳聾有關,其研究團隊正在嚐試的多個靶點基因在動物模型上也初見療效,OTOF是第一個走上人體臨床試驗的。
在這項臨床研究中,舒易來團隊採用耳部注射的方式,實現了雙載體AAV藥物治療先天性耳聾的全球首批臨床給藥。舒易來解釋,之所以採用雙AAV載體遞送,是因為OTOF基因比較大,超過了AAV載體的裝載容量,“打個比方,一輛車搬不動它,需要兩輛車一起搬,藥物注射入人體後,這兩輛車就合併起來,形成了一個完整的基因。”
據悉,該研究納入的第一批患者年齡為3-10歲,在確認安全性和有效性後,研究團隊逐步放寬年齡限制,第二批患者招募時,1-3歲符合條件的患者也可以入組。舒易來表示,這項工作的開展離不開醫院的大力支持,也離不開科主任李華偉教授的帶領和一直以來的支持。
該臨床試驗從2022年10月開始正式啟動患者招募,“招募信息發出後,當天就有好多人來聯繫我們。我們從中篩選出幾位患者,都是耳聾程度特別嚴重,對聲音沒有反應的兒童。之所以選擇這類兒童,是因為用藥的效果在他們身上會被反映得更加容易判斷。針對第一批患者,我們也更加註重安全性。” 舒易來說。
未來將繼續隨訪
2022年12月28日,在李華偉教授的帶領和支持下,舒易來團隊進行了全球第一例先天性耳聾患兒的基因治療,目前,該患兒的聽力恢復已經持續了10個月。在安全性方面,舒易來表示:“局部注射大大降低了發生潛在風險的可能性,同時我們使用的劑量也很低。”
值得關注的是,招募的5位患兒中有1位的聽力沒有成功得到改善,舒易來分析了可能的原因:“我們發現這個兒童體內的AAV載體抗體水平比別人高很多,說明他以前可能接觸過AAV。”
AAV雖然是一種免疫原性很低的載體,但仍然會引起人體的免疫反應。有數據顯示,40%-80%的成人曾經曆過AAV感染,人體內已經存在的針對AAV的中和抗體,成為AAV載體遞送的一項可能的重大挑戰。對此,舒易來表示,團隊在手術前會檢查患者體內的抗體水平,如果他/她曾經對AAV暴露過,相應抗體水平過高,就不會被納入試驗組。另一方面,目前臨床試驗中的兒童均只在一隻耳朵中注射了RRG-003,而注射過RRG-003後,患兒體內也會產生抗體,另一隻耳朵的注射可能要等很長一段時間。
為確保安全性和有效性,舒易來團隊計劃對這兩批首先入組的患者繼續觀察,如果可能的話,會一直隨訪下去。同時,其研究團隊也正在開發一些針對其他耳聾基因的基因療法。希望有更多新的治療藥物被研發出來,讓更多患者回到有聲世界。
目前,全球已上市的基因療法大多定價昂貴,普通家庭幾乎難以負擔。舒易來表示,解決這一問題的一種方式是納入醫保,另一個辦法是按年付費。同時,整個醫學界和產業界要共同努力降低成本,從而降低價格,惠及更多的患者。